健康客戶端不完全統計,7月美國食品和藥物管理局(FDA)共批準6款新藥,歐洲藥品管理局暫無新增推薦上市藥品;我國國家藥品監督管理局僅批準1款1類創新藥。醫療器械方面,美國食品和藥物管理局首次批準PMA器械1個,我國3個三類醫療器械獲批上市已公示。
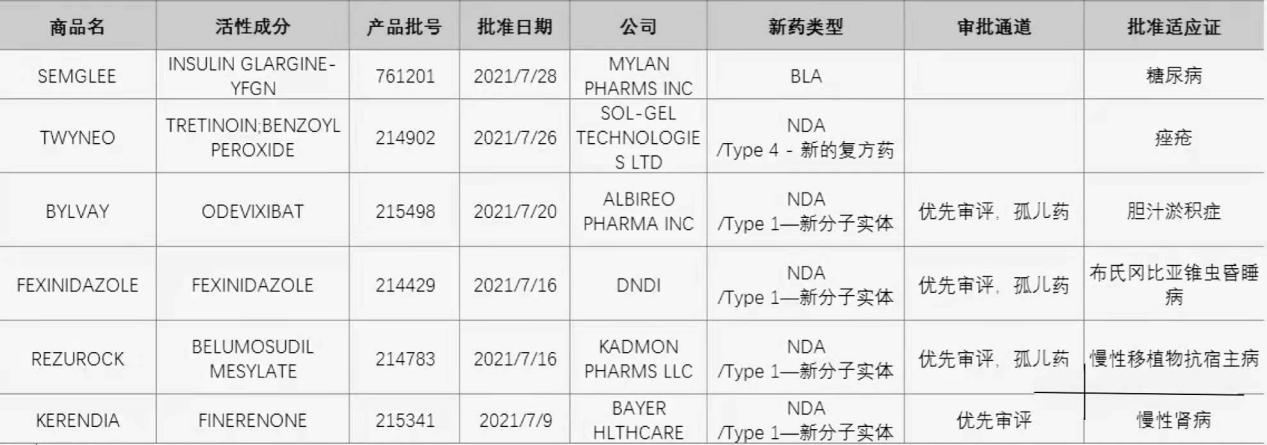
截至7月30日,美國食品和藥物管理局共批準6款新藥,其中包括4款新分子實體藥物、1款生物制品藥物。Mylan公司的Semglee(甘精胰島素-yfgn ),是首款可替代的糖尿病生物仿制胰島素,其批準可能有助于胰島素藥品價格的降低。
據FDA網站信息,截至7月30日,共有1個通過上市前批準(PMA)途徑首次上市,為免疫學和微生物學器械,獲批日期為7月14日。
據國家藥品監督管理局網站公開信息,截至7月30日,本月僅有1款1類創新藥獲批,是河南真實生物科技有限公司生產的阿茲夫定片,為優先審評的附條件批準化藥,適應癥為艾滋病,批準文號是國藥準字H20210035\H20210036。
阿茲夫定片作為全球首款雙靶點抗HIV-1上市創新藥,是國內具有自主知識產權的口服抗HIV-1新藥,將為HIV-1感染者提供了新的治療選擇,且國家藥監局已經批準其用于治療新冠肺炎的Ⅲ期臨床試驗。
截至7月30日,國家藥品監督管理局網站公示了3個三類醫療器械獲批上市,分別為:賽諾醫療科學技術股份有限公司的顱內藥物洗脫支架系統、天津市鷹泰利安康醫療科技有限責任公司的陡脈沖治療儀和百康芯(天津)生物科技有限公司的呼吸道病原菌核酸檢測試劑盒(恒溫擴增芯片法)。







 CopyRight ? 2013-2022 Brand food.cn All Rights Reserved.
CopyRight ? 2013-2022 Brand food.cn All Rights Reserved.